Qu’est-ce que le pH ?
Le pH est une valeur qui permet de savoir si une solution est acide, neutre ou basique. C’est une échelle de mesure comprise entre 0 et 14. On peut le comparer à un « thermomètre chimique ».
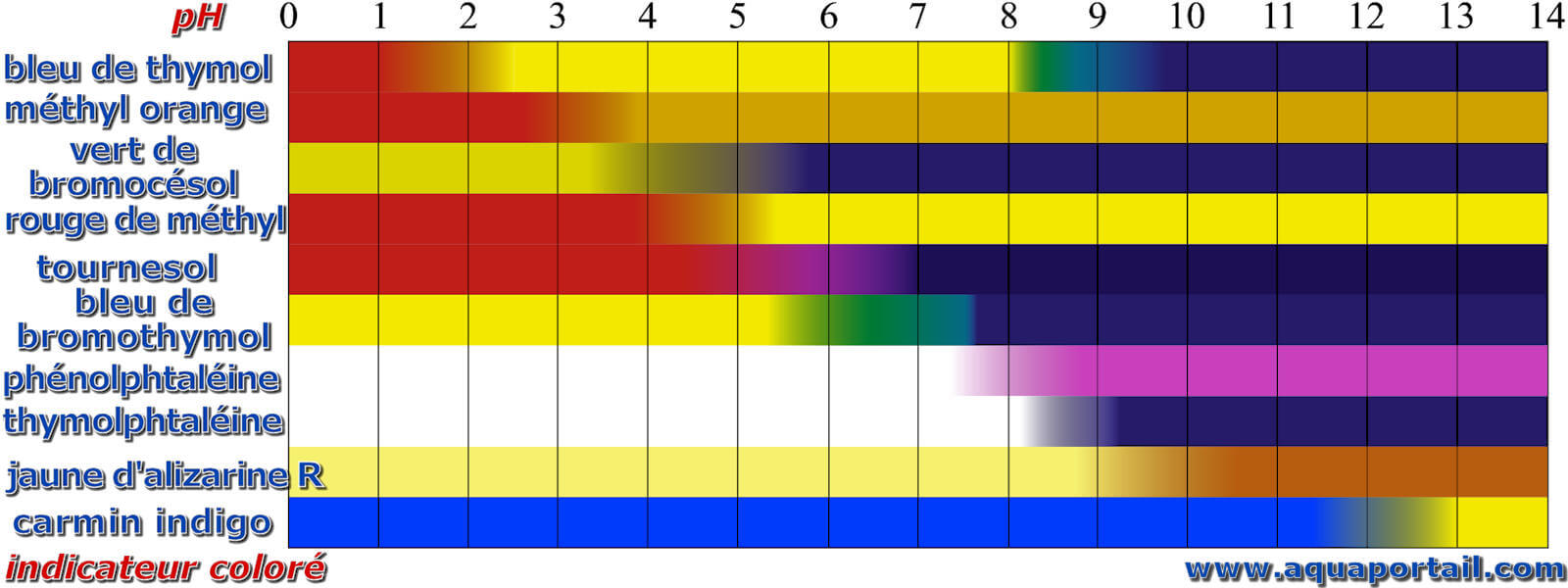
L’échelle du pH
- Un pH de 7 correspond à une solution neutre, comme l’eau pure.
- Un pH inférieur à 7 indique une solution acide. Plus la valeur se rapproche de 0, plus l’acidité est forte.
- Un pH supérieur à 7 indique une solution basique (ou alcaline). Plus la valeur se rapproche de 14, plus la basicité est forte.
Exemple :
- Le jus de citron a un pH ≈ 2 (acide).
- L’eau du robinet a un pH proche de 7 (neutre).
- Le savon a un pH ≈ 9 (basique).
Le pH dans la vie quotidienne
Le pH de l’eau que nous buvons doit être proche de 7 afin de ne pas être trop acide ni trop basique. Chaque liquide de notre quotidien possède son propre pH : salive, boissons, produits ménagers...
À retenir
- Entre quelles valeurs varie le pH ?
- Que signifie un pH de 7 ?
- Comment distingue-t-on une solution acide d’une solution basique ?
- Quel est le pH idéal de l’eau de consommation ?